- 2021/07/09 掲載
NTTデータとファイザー、臨床研究における業務効率化に向けた共同研究を開始
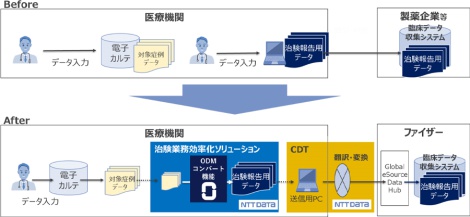
臨床研究では、新薬等の効果と安全性を検証するためにALCOA(Attributable:帰属性、Legible:判読性、Contemporaneous:同時性、Original:原本性、Accurate:正確性)が担保された臨床データの収集が不可欠です。また、一般的に臨床データは、電子カルテを含む複数の原資料(研究の事実経過の再現と評価に必要な記録)から収集されます。電子カルテのデータを原資料として利用する場合、医療機関では電子カルテおよび臨床データ収集システム(EDC:Electronic Data Capture)への入力作業が必要で、重複した作業が発生しています。
本共同研究では、電子カルテのデータを国際標準に準拠して効率的に変換・転送するソリューションを開発し、重複する入力作業とデータ点検作業の大幅な軽減を含む医療機関・製薬企業双方に有益な新しい臨床研究の仕組みの実現を目指します。この治療と臨床研究の橋渡しは国際的に関心をもって取り組まれている課題であり、今回、国立がん研究センター東病院が協力医療機関として共同研究を推進します。
新型コロナウイルス感染症流行拡大を経験し、治療・臨床研究等のスピード感を伴った更なる高品質かつ効果的な実施は、ニューノーマルの要請となりました。本共同研究により、デジタル技術を活用した新たな取り組みを加速させ、患者さんに貢献していきます。
■背景
患者さんに新たな治療法をお届けするための臨床研究を含む医薬品の開発は、長い年月(平均12-15年)と費用(約26億ドル)(注1)を要します。また、世界的なパンデミックによる制約等により、臨床研究等における医療機関側の管理上の負担や、製薬企業側の原資料確認などに影響が出ており、その実施方法について改善が必要となっています。このような背景から、医療機関および製薬企業双方において、より効率的で高品質かつ迅速な臨床研究の新しい手法に対するニーズが高まっています。
このニーズに応えるために、本共同研究では重複入力作業の軽減やデータ点検作業の大幅な削減を含む革新的な臨床研究の実現に向けた新しい手法を開発します。このソリューションには、医療機関の電子カルテ環境内にある臨床データを臨床研究報告用データに変換した上で、CDTサービス(注2)等のプラットフォームを用いてデータを処理し、製薬企業等が管理するEDCに登録する機能を備えています。
注1 1.Eisenstein, E.L., et al., Reducing the costs of phase III cardiovascular clinical trials. Am Heart J, 149(3) (2005) 482-488
2.Joseph A. D., et al., Innovation in the pharmaceutical industry: New estimates of R&D costs. J Health Econ, 47 (2016) 20-33
注2 Clinical Data TransferTMサービスの略称。医療機関から製薬企業への臨床データファイルの転送およびデータ翻訳、用語変換を実施するサービスです。医療分野で豊富な実績を有するセキュアな共同利用型ネットワーク基盤を採用し、各種データのトレーサビリティーを確保した形で提供しています。本サービスはNTTデータとファイザーが本共同研究に先立って2社で実施した研究活動の成果からNTTデータが開発し、2020年12月よりサービス提供しています。
https://www.nttdata.com/jp/ja/news/services_info/2020/110500/
PR
PR
PR